واکنش اصلی در سنتز پپتیدها، کوپلینگ میان دو آمینواسید است. آمینواسیدها با از دست دادن یک مولکول آب با یکدیگر کوپل می شوند تا دی پپتید موردنظر را تشکیل دهند. این فرآیند خود به خود اتفاق نمیافتد، آنها باید فعال شوند تا واکنش رخ دهد. برای این منظور، معرفهای جفتکننده ساخته شدهاند. آنها آمینواسیدها را به مشتقات واکنش پذیرتری تبدیل میکنند و آبی را که به طور همزمان در سیستم تشکیل میشود را حذف میکنند.
مثال زیر نمونهای از یک دیپپتید، متشکل از دو آمینواسید مختلف می باشد:
L-Alanyl-L-phenylalanine (H-Ala-Phe-OH)
با این حال، اگر یک معرف جفتکننده به مخلوطی از آلانین و فنیل آلانین اضافه شود، منجر به سنتز چهار دی پپتید متفاوت میشود. پپتیدهای سه آمینواسیدی و طولانیتر نیز ممکن است تولید شوند. برای به دست آوردن دیپپتید مورد نظر H-Ala-Phe-OH و نه مخلوطی از پپتیدها، دو گروه محافظ مورد نیاز است. آنها نباید تحت شرایط واکنش کوپلینگ از آمینواسید جدا شوند، اما می بایست پس از انجام کوپلینگ به راحتی در یک مرحله مجزا، جدا گردند.
گروه آمینی آلانین باید محافظت شود:
H-Ala-OH → X-Ala-OH
و همچنین گروه اسیدی فنیلآلانین نیز باید محافظت گردد:
H-Phe-OH → H-Phe-OY
اکنون فقط گروه اسیدی آلانین می تواند با گروه آمینی فنیل آلانین واکنش دهد:
X-Ala-OH + H-Phe-OY → X-Ala-Phe-OY
در نهایت، گروه های محافظ تحت شرایط یکسان حذف میشوند:
X-Ala-Phe-OY → H-Ala-Phe-OH
برای اینکه پپتیدهای طولانیتری را بتوان سنتز کرد باید X و Y به گونه ای انتخاب شوند تا X تحت شرایطی که OY حفظ میشود، حذف شود. به مثال زیر توجه کنید:
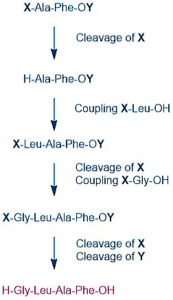
X یک گروه محافظ موقت نامیده میشود زیرا فقط برای مرحله کوپلینگ استفاده میشود. Y یک گروه محافظ دائمی است. Y باید به اندازه کافی پایدار باشد تا تمام مراحل کوپلینگ و محافظت زدایی X را تحمل کند. با این وجود باید در مرحله آخر، بدون آسیب رساندن به پپتید، قابل حذف باشد. یک پپتید همیشه دو گروه مختلف در هر انتها دارد و در نتیجه یک “جهت” دارد. گروه آمینی در انتهای یک پپتید به عنوان N-ترمینال و گروه کربوکسیل در انتهای دیگر C-ترمینال شناخته میشود. در سنتزهای شیمیایی، پپتید از C-ترمینال در جهت N-ترمینال ساخته میشود و بنابراین گروه C-ترمینال باید در کل سنتز محافظت شود.
گروه های محافظ برای اطمینان از جهت توالی آمینواسیدها ضروری هستند.
گروه های محافظ اصلی مورد استفاده برای محافظت α-آمین (Nα) آمینواسیدها شامل Fmoc (9-Fluorenylmethoxycarbonly)، Boc (t-Butoxycarbonyl) و Z (Benzyloxycarbonyl) میباشد. هر یک از آنها استراتژی کلی سنتز پپتید را تعریف میکنند و بنابراین، شرایط حفاظت و محافظتزدایی مطابق با آنها تغییر خواهد کرد. Fmoc در شرایط اولیه با شستشوی پیپپریدین حذف میشود، در حالی که Boc به شرایط اسیدی مانند شستشوی تری فلورواستیک اسید نیاز دارد و Z با هیدروژناسیون کاتالیزوری روی/پالادیوم حذف میشود.
بنزیلوکسی کربونیل (Z) یا (Cbz) قدیمی ترین گروه قابل استفاده برای محافظت از Nα آمینواسیدها است. توسعه Z باعث شروع سنتز پپتیدهای مدرن شد و مخفف Z به افتخار لئونیداس زرواس به این گروه محافظتکننده اختصاص داده شد. امروزه گروه Z هنوز هم برای محافظت از گروه آمینی در واکنشهای آلی استفاده می شود. برخلاف گروه α-آمینی، گروه اسید پایانی باید در کل سنتز محافظت شود. متداولترین گروههای محافظ و شرایط محافظتزدایی آنها در جدول زیر نشان داده شدهاست:
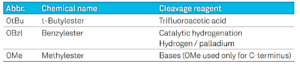
علاوه بر آمین الفا و گروه اسیدی آمینواسیدها، زنجیره های جانبی نیز باید محافظت شوند تا از هرگونه واکنش جانبی در این موقعیت در طول واکنش کوپلینگ جلوگیری شود. در واقع، اگر یک گروه واکنش پذیر در زنجیره جانبی وجود داشته باشد، به عنوان مثال، اسید آمینه لیزین، می تواند در مرحله کوپلینگ واکنش دهد و منجر به تشکیل انشعابات و محصولات جانبی ناخواسته شود.
انتخاب گروههای محافظ آمین و کربوکسیل به روش و استراتژی سنتز بستگی دارد. دو روش مهم در بخش بعدی توضیح داده شده است.
فاز جامد یا فاز مایع؟ دو روش مختلف اما مکمل!
دو روش استاندارد برای سنتز پپتید وجود دارد: سنتز پپتید فاز جامد (SPPS) و سنتز محلول (LPPS). جدول زیر شباهت ها و تفاوت های بین این دو روش را خلاصه میکند.
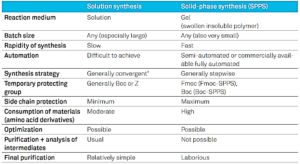
سنتز محلول هنوز برای سنتز برخی از پپتیدهای بسیار کوتاه (مانند دی پپتیدها) و پپتیدهای اصلاح شده در C-ترمینال انتخاب میشود. مزایای اساسی سنتز فاز جامد نسبت به سنتز محلول، سرعت و سهولت انجام آن است. با این حال، اغلب گفته می شود که هر چه مقیاس سنتز بزرگتر باشد، SPPS آهستهتر پیش میرود، زیرا “کار دستی” افزایش مییابد. اما در مقیاسهای کوچک و متوسط می توان پپتیدها را در یک ماشین کاملاً اتوماتیک همانطور که در تصویر زیر نشان داده شده است، تولید کرد.

مقادیر بسیار زیاد (چند کیلوگرم پپتید) در ماشینهای نیمه خودکار (فقط برنامه شستشو به طور خودکار اجرا میشود) یا به صورت دستی تولید میشوند. این فرآیند همیشه شامل چهار مرحله تکراری است:
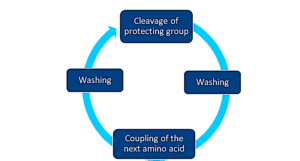
یک پروتکل استاندارد برای SPPS وجود دارد که برای سنتز اکثر پپتیدها عمل میکند در حالی که سنتز محلول نیاز به برنامهریزی دقیق تری دارد و چنین پروتکلی برای سنتز در فاز محلول وجود ندارد. سنتز در فاز محلول نه تنها در انتخاب گروههای محافظ بلکه در روشهای کوپلینگ، حلال های مورد استفاده و روشهای آماده سازی نیز تفاوت های زیادی با SPPS دارد.